Сперматозоиды из стволовых клеток. Внуки стволовой клетки. Цитокины и факторы роста
Ученым из Йокогамы удалось ранее невозможное: вырастить жизнеспособные искусственные сперматозоиды. Половые клетки "из пробирки" помогут бесплодным парам, где мужчина страдает некроспермией, завести детей. Этот недуг часто является результатом облучения - так что для Японии, пережившей трагедию "Фукусимы", данная проблема может стать особенно актуальной.
Недавно японские ученые из Университета Йокогамы опубликовали результаты своих последних экспериментов по созданию искусственных сперматозоидов. По их заявлению, испытания прошли успешно - большинство получившихся мужских половых клеток были абсолютно "работоспособны", и когда их "познакомили" с яйцеклетками, то сразу же приступили к оплодотворению. Причем дети, получившиеся в результате подобного процесса, родились совершенно здоровыми.
Правда, сразу хочу огорчить тех, кто подумал, что теперь-то мужчины уж точно будут лишними на нашей планете - речь идет не о человеческих, а о мышиных сперматозоидах. Да и искусственными на самом деле их назвать достаточно сложно - ведь данные половые клетки не были созданы людьми, словно знаменитая микоплазма Крейга Вентера, от начала и до конца. Они были выращены из предшественников мужских половых гамет (сперматоцитов первого порядка), однако это произошло не в организме мышей-самцов, а в лабораторных условиях (или, как говорят неспециалисты, "в пробирке").
До сих пор подобного не удавалось достичь вне живого организма. Сперматоциты первого порядка в искусственных условиях чувствовали себя хорошо, но вот делиться с помощью мейоза (деления, в результате которого из клеток с двойным набором хромосом получаются таковые с одинарным) никак не желали. А если вдруг и начинали, то делали это, что называется, "вкривь и вкось", в результате чего 80% получившихся сперматозоидов оказывались непригодными к оплодотворению, а оставшиеся, хоть и могли сделать это, но все же приводили к рождению мышат с разными генетическими дефектами.
Почему преодолеть "мейозный барьер" оказалось так сложно? Для того, что бы понять это, следует вспомнить, что представляет собой данная разновидность деления. Как мы помним, перед делением обычной клетки ее набор хромосом удваивается, и непосредственно перед процессом становиться не двойным, а четверным. После чего клетка делится на две, каждая из которых содержит двойную порцию хромосом.

А вот при мейозе все происходит куда сложнее - сначала сперматоцит первого порядка делиться как обычная клетка, на два сперматоцита второго порядка, которые, как им и положено, обладают двойным набором хромосом. Практически сразу, не удваивая своего ДНК, они делятся на четыре сперматозоида с одинарной порцией наследственного вещества у каждого. При этом все это происходит, что называется, "на автомате", ведь никакого генетического контроля со стороны клеточного ядра при его делении быть не может (с ДНК, которая свернута в хромосому, невозможно считать информацию).
А если дело обстоит так, то все внешние условия, в которых происходит этот сложный процесс, должны быть абсолютно стабильными. Любое изменение температуры, влажности или кислотности сразу же приведет к нарушению работы механизма деления, а то и к полной остановке сперматогенеза. Именно поэтому долгое время и не удавалось запустить мейоз "в пробирке" - даже при современных технологиях ученым достаточно сложно соблюдать данное правило. Однако аккуратным и пунктуальным японским эмбриологам, судя по всему, это удалось.
Группа ученых во главе с доктором Такехико Огава для проведения эксперимента воспользовались клеточной культурой, взятой из семенников лабораторных мышей. Поскольку она храниласьв замороженном виде, сначала пришлось аккуратно и медленно разморозить их, после чего они были помещены в идеально подобранные условия, напоминавшие таковые внутри половых желез грызунов. Процесс "созревания" сперматозоидов длился достаточно долго - около 2-х месяцев (в организме мышей это происходит быстрее). Из полученных гамет больше половины оказались абсолютно нормальными.
После этого получившихся "микрофранкенштейнов" ввели самкам мышей, которые сразу же забеременели. В итоге все они родили здоровых мышат, которые, как это выяснилось впоследствии, также произвели на свет абсолютно здоровое потомство. Это говорит о том, что эксперимент по созданию искусственных сперматозоидов увенчался полным успехом.
Исследователи считают, что через какое-то время будет вполне возможно создавать таким же образом искусственные сперматозоиды человека. Это поможет бесплодным парам, где мужчина страдает некроспермией (дефект организма, при котором сперматогенез идет не правильно и гаметы получаются нежизнеспособными) наконец-то завести детей. Кстати, поскольку некроспермия часто является результатом радиоактивного облучения, для нынешней Японии, пережившей катастрофу на АЭС "Фукусима", эта проблема может стать особенно актуальной.
Однако данный метод позволяет получать искусственные сперматозоиды из их предшественников, то есть из половых клеток. Но если вдруг и они в человеческом организме окажутся дефектными? Можно ли будет сделать гаметы из обычных клеток организма. Многие эмбриологи считают, что да.

Два года назад сотрудникам Медицинской школы Стэнфордского университета (США) уже удалось "уговорить" эмбриональные стволовые клетки человека стать клетками-предшественниками яйцеклеток и сперматозоидов. Группа эмбриологов под руководством доктора Рене Рейхо Пера обработали стволовые клетки, полученные из человеческих эмбрионов белками, которые стимулируют образование гамет. Кроме того, В дополнение к этому стволовые клетки были избавлены от метильных групп своих ДНК, которые наделяют их конкретными чертами, препятствующими способности клеток становиться предшественниками гамет.
Одновременно ученым удалось стимулировать работу генов DAZ и BOULE, которые как раз и регулируют процесс образования половых клеток. В результате одновременная высокопродуктивная работа всех этих генов позволила эмбриологам создать клетки с одинарным набором хромосом, то есть практически сперматозоиды и яйцеклетки. Правда, настоящими мужскими гаметами в итоге стали лишь 2% стволовых клеток, а нормальную яйцеклетку получить так и не удалось.
30 Октября 2009От бесплодия спасут искусственные половые клетки
Алексей Тимошенко, GZT.ru
Биологам впервые удалось получить половые клетки из эмбриональных стволовых. Это крайне важный шаг в получении искусственной спермы и яйцеклеток, ведь в перспективе именно с их помощью будут лечить бесплодие.
Группа ученых из Стэнфордского университета (США, штат Калифорния) опубликовала в журнале Nature , в которой рассказала о получении из эмбриональных стволовых клеток человеческих гамет – половых клеток. Об их непосредственном применении в репродуктивной медицине говорить преждевременно, хотя теоретически работа биологов может привести к радикальному решению проблемы бесплодия.
Бесплодие: окончательное решение вопроса?
Бесплодие у человека может быть вызвано целым рядом причин. Сложный и деликатный процесс формирования яйцеклеток и сперматозоидов зависит от сотен, если не тысяч факторов, и в настоящее время далеко не всегда удается справиться с его нарушениями.
Открытие стволовых клеток и последующее изучение их свойств дает определенную надежду на решение деликатной проблемы. Стволовые клетки могут неограниченно делиться и впоследствии приобретать различную специализацию, давая начало самым разным тканям и органам. Так почему бы их не использовать и для получения в лабораторных условиях половых клеток? Ведь репродуктивные органы формируются в конечном итоге всего из их нескольких штук!
Если в пробирке удастся вырастить из стволовых клеток сперматозоиды или яйцеклетку, главное – чтобы будущая мама смогла выносить подсаженный в матку эмбрион. Или можно прибегнуть к суррогатному материнству: тогда детей смогут иметь даже те пары, которые столкнулись с самыми тяжелыми нарушениями репродуктивной функции – отсутствием матки, яичников или семенников.
Впрочем, выращивать яйцеклетки и сперматозоиды из клеток, которые изначально половыми не являются, только предстоит научиться. Еще нужно будет понять, как перепрограммируется стволовая клетка, изучить возможные риски, отработать множество разных методов – именно над этими проблемами сейчас и работают ученые.
Прогресс не стоит на месте
О работах в области искусственных гамет в GZT.RU уже рассказывалось: летом 2009 года ученым из США удалось вырастить яйцеклетку из незрелого фолликула (пузырька внутри яичника, где формируется яйцеклетка в нормальных условиях), а их британские коллеги даже прошли весь путь, от стволовой клетки до сперматозоида.
И вот сделан новый шаг. Калифорнийская группа исследователей идентифицировала гены, воздействуя на которые удалось направить стволовые клетки по пути формирования гамет. Гены, обозначенные как DAZ и BOULE, оказались необходимы для мейоза – специфического для образования половых клеток процесса.
Обычные клетки делятся митозом: пополам и с получением каждой дочерней клеткой двойного комплекта ДНК. Половые же клетки образуются путем мейоза – делением два раза подряд с получением в итоге четырех клеток с одинарным комплектом генетического материала. При слиянии сперматозоида и яйцеклетки снова получается клетка, несущая двойной набор ДНК, и в дальнейшем уже она начинает делиться митозом.
Хотя ученые использовали эмбриональные стволовые клетки, прогресс в области получения стволовых клеток позволяет надеяться на то, что со временем удастся отработать и достаточно надежные методики получения стволовых клеток из обычных. В таком случае у пациента можно будет взять крошечный кусочек кожи или иной ткани, выделить из него группу клеток, превратить их в стволовые, потом провести еще одну манипуляцию – и получить сперматозоиды или яйцеклетки.
Описанные многостадийные манипуляции сейчас кажутся крайне сложными. Ученые подчеркивают, что их работа «значительна с точки зрения дальнейших научных исследований в этой области», и только потом добавляют осторожное: «И потенциальных клинических применений». Подводных камней на пути решения проблемы бесплодия еще очень много, но движение вперед продолжается, и это исследование – тому наглядное свидетельство.
назадЧитать также:
08 Июля 2009Сперма из стволовых клеток
Британские исследователи создали стратегию получения в пробирке мужских сперматогенных клеток-предшественниц (germline stem cells – GSCs) из человеческих эмбриональных стволовых клеток.
читать 15 Апреля 2009Сперма-рекордсмен
По словам врачей американской клиники, проводивших процедуру ЭКО, 22 года между моментом сдачи образца спермы в 1986 году и оплодотворением в 2008 – это мировой рекорд.
читать 06 Апреля 2009Мужская контрацепция: надо расслабить хвостик
Белок CATSPER1 – часть ионного канала, запускающего внутрь клетки ионы кальция. В результате хвостик сперматозоида начинает биться с усиленной энергией. В отсутствие этого белка сперматозоиду просто не хватает сил, скорости и подвижности оплодотворить яйцеклетку. Это же состояние Смит и его коллеги предлагают вызвать искусственно, заблокировав кальциевые каналы с помощью лекарственных препаратов.
читать 24 Октября 2008Что влияет на качество спермы
Для мужчин есть две новости: плохая и хорошая. Плохая состоит в том, что на качество спермы влияет практически все, хорошая – все поправимо.
читать 14 Июля 2008Хотите детей? Боритесь с ожирением!
Для мужчин, страдающих ожирением, характерен малый объем семенной жидкости и повышенное относительное содержание аномальных сперматозоидов.
Стволовые клетки – это дифференцированные клетки тела, которые имеют свойство трансформироваться в любые другие функционально активные клетки. Они присутствуют практически во всех органах и тканях. Если в организме возникают какие-либо повреждения, автоматически происходит мобилизация стволовых клеток, после чего они с кровотоком направляются к нужному органу и там заменяют поврежденные волокна.
Стволовые клетки являются «универсальными». При необходимости они могут приобретать свойства и функции клеток любого типа тканей. Стоит отметить, что количество данных клеток в организме ограничено, поэтому при слишком сильных, множественных поражениях, организм не сможет осуществить полноценный «ремонт».
Стволовые клетки давно заинтересовали ученых. На данный же момент проходит множество исследований в данной сфере. Медики надеются при помощи их научиться лечить тяжелые патологии, в том числе и некоторые формы бесплодия.
Для забора стволовых клеток обычно используется:
- Костный мозг. Операция проходит под общим наркозом, поэтому пациент не ощущает какой-либо дискомфорт.
- Периферическая кровь. При этом отбираются только стволовые клетки, а другие составляющие крови возвращаются обратно организм. Данная процедура обычно проводится в амбулаторных условиях.
- Жировая ткань. Процедура забора жира относится к самым малотравматичным.
- Кровь из пуповины. Ее собирает акушерка. Никакой опасности для матери и новорожденного это не несет. Сбор стволовых клеток можно осуществлять вне зависимости от способа родов (самостоятельные или при помощи кесарева сечения).
Для выполнения медицинских манипуляций можно применять стволовые клетки, как самого больного, так и донорские. При этом донором может быть как родственник, так и абсолютно посторонний человек. То, насколько процедура окажется эффективной, будет напрямую зависеть от совместимости доноров и от индивидуальных особенностей организма человека.
После забора клеток их отправляют в лабораторию. Там происходит их размножение. Прежде чем трансплантировать данные клетки, специалисты проверяют их на наличие вирусов и патогенных бактерий. Если пациент в ходе терапии будет придерживаться рекомендаций лечащего врача, излечение должно будет наступить в самые короткие сроки.
Применение
Если у пациента бесплодие – стволовые клетки могут вводиться разными способами, например:
- ангиографическим – выполняется при помощи катетера;
- внутривенным;
- интратекальным – введение в спинномозговой канал;
- хирургическим – клетки вводятся непосредственно в очаг поражения.
Иммунитет
Лечение стволовыми клетками благоприятно влияет на иммунитет, поэтому если причиной бесплодия у пациента (женщины или мужчины) является перенесенный в прошлом воспалительный процесс, инфекционное заболевание, сбои в иммунитете или стресс, то оно сможет дать превосходные результаты.
Например, если бесплодие вызвал простатит, то такое лечение спровоцирует рассасывание спаек, возникших в районе простаты. Дело в том, что после введения стволовых клеток в организм они направляются к очагу патологического процесса и там воссоздают новую сеть здоровых сосудов. В свою очередь это приводит к восстановлению работы рецепторов, которые находятся в сосудистых стенках и в простате.
Все это препятствует застойным явлениям в предстательной железе. Помимо этого стволовые клетки способствуют восстановлению поврежденных тканей яичек и придатков, улучшают работу защитных сил организма, что крайне важно для борьбы с инфекцией. Таким образом, происходит нормализация работы эндокринной системы, улучшение показателей эякулята.
Для лечения простатита стволовые клетки берутся из позвоночника, а затем выращиваются в течение 40-60 дней. После этого средство вводится пациенту в вену инъекционным способом. Спустя полгода процедура повторяется.
Эндометрий
В течение месяца тело женщины подвергается воздействию половых гормонов, в результате чего происходит рост слизистой оболочки матки. При этом эндометрий становится максимально подходящий для имплантации оплодотворенной яйцеклетки и дальнейшего вынашивания плода.
Однако так происходит далеко не всегда. При эндокринных нарушениях и воспалительных процессах в органах малого таза, эндометрий плохо развивается, в результате чего плодное яйцо не может к нему прикрепиться. Как показывает практика, у 60-65%женщин, имеющих патологии эндометрия наблюдается бесплодие, а если беременность и наступает, то она вскоре заканчивается выкидышем.
К счастью, современные ученые нашли способ решения данной проблемы. Благодаря стволовым клеткам женщина теперь сможет зачать и выносить ребенка даже с тяжелыми патологиями эндометрия. В данном случае забор стволовых клеток происходит из жировой ткани пациентки. После обработки и выращивания в лаборатории их помещают в матку.
Таким образом, происходит быстрое восстановление эндометрия, а также обновление ооцитов. Данный процесс длится не больше 2 недель. На протяжении всего лечения женщине регулярно делают УЗИ. После достижения эндометрием нормальных показателей, проводится процедура ЭКО.
Метод уже был опробован на 40-летней пациентке, которая имела серьезные патологии эндометрия и на протяжении длительного времени не могла зачать ребенка. С ее диагнозом еще никому не удавалось забеременеть, однако израильские врачи створили настоящее чудо. Пациентка не только забеременела, но и выносила, успешно родила здорового малыша.
К основным преимуществам такой процедуры можно отнести ее простоту и в то же время высокую эффективность. Ученые утверждают, что с помощью стволовых клеток можно решить проблему бесплодия в 85% случаев. А это весьма неплохой показатель.
Истощения яичников
В данном случае терапия стволовыми клетками нередко комбинируется с различными методиками традиционной китайской медицины.
Сам план лечения выглядит примерно так:
- Терапия стволовыми клетками. Женщине постепенно вводится 4 инъекции. Забор стволовых клеток происходит в области бедра (это занимает 30-60 минут), после чего их выращивают в лаборатории в течение 2-3 недель, а затем вводят обратно в тело пациентки инъекционным способом. Данные стволовые клетки будут восстанавливать половые клетки.
- Традиционная китайская медицина. Она включает в себя иглоукалывание. Проводится оно 5 раз в неделю. Исключением может быть только период месячных. Таким образом, происходит создание наилучших условий для роста клеток в организме.
- Туина. Это особая техника лечебного массажа. Выполняется он 5 раз в неделю. Исключением являются дни менструации.
- Поддерживающая терапия.
- Китайское лечение средствами, изготовленными на основе лекарственных растений. Длится оно на протяжении 3 месяцев.
Непосредственно сам период лечения стволовыми клетками продолжается 30 дней. Он происходит в медицинском учреждении. Традиционное китайское лечение, а также иглоукалывание выступают в роли вспомогательного средства.
После такого лечения работа яичников улучшается, стабилизируется гормональный фон, нормализуется работа нервной системы.
Создание гамет
Как выяснилось, в скором времени для продолжения рода людям не понадобятся репродуктивные клетки, выработанные их репродуктивными органами. Ученые научились создавать яйцеклетки и сперматозоиды искусственным путем.Это значит, что в медицине может произойти настоящий прорыв лечении бесплодия. Благодаря искусственным репродуктивным клеткам детей смогут иметь люди, которые в прошлом прошли курс химиотерапии или облучение во время лечения онкологии.
Выращивание половых клеток происходило в Калифорнийском университете. Для этих целей использовались стволовые клетки эмбрионов. Медики создали уникальный препарат, который состоит из витаминов и различных химических веществ. С его помощью и происходит преобразование стволовых клеток в сперматозоиды и яйцеклетки.
Готовые сперматозоиды оказались вполне пригодными для дальнейшего оплодотворения женской яйцеклетки. В то же время женские половые клетки остались на начальном этапе развития, в результате чего оплодотворение их было невозможным.
Однако ученые не отчаиваются и не планируют останавливаться на достигнутом. В дальнейшем они планируют создать репродуктивные клетки из клеток, взятых из кожи человека.
Данные клетки планируют поместить в особый раствор, в котором их биологическое время переведется до эмбрионального состояния, а затем из них получат «мужскую яйцеклетку» и «женский сперматозоид».
Стоит отметить, что такое заявление ученых вызвало в обществе множество разногласий в плане морали и этики. Если ученым удастся создать искусственные половые клетки, то в будущем у людей может исчезнуть желание самостоятельно продолжать род. Религия также не приветствует такое вмешательство в интимный процесс.
Противники данного эксперимента утверждают, что стволовые клетки могут использоваться в более нужных направлениях. Например, для терапии тяжелых болезней, выращивания внутренних органов в лабораториях.
Побочные эффекты
Возможно, в скором будущем стволовые клетки и займут почетное место в терапии всевозможных заболеваний, в том числе и тех, которые вызывают бесплодие. Однако на данный момент эта отрасль медицины находится в стадии начального развития и поэтому первые попытки терапии часто приводят к осложнениям.
Так, способность стволовых клеток быстро делиться может провоцировать рост доброкачественных и злокачественных опухолей в теле. Такой побочный эффект долгое время не был доказан. Однако в 2005 году специалисты одной из израильских клиник наблюдали стремительное развитие раковых опухолей в головном и спинном мозге у мальчика, после того как в Москве для лечения генетической болезни ему делали инъекции стволовых клеток. Специалисты центра «Шиба» доказали, что рост опухоли и инъекции стволовых клеток в данном случае связаны.
Кроме этого в последнее время участились смерти звездных пациентов (среди таких Илья Олейников, Жанна Фриске), которые прибегали к терапии стволовыми клетками. Все это шокировало общественность.
Важно сказать, что помимо канцерогенного эффекта, стволовые клетки могут оказывать еще аллергическое, токсическое и генетическое воздействие. Механизм работы стволовых клеток до конца не изучен, поэтому обращаться к подобному методу терапии без особой необходимости не рекомендуется.
Конечно, это еще не значит, что лечение стволовыми клетками бесперспективное занятие. Скорее должно пройти время, закончиться многочисленные эксперименты по введению средства животным и людям. Только после этого можно будет сказать, что лечение бесплодия стволовыми клетками является самым эффективным и безопасным.
Кожа с возрастом неизбежно меняется по структуре. Однако, косметология уже достигла уровня, когда в некоторых вопросах способна поспорить с природой, используя ее же ресурсы. Выясняем, с помощью каких средств можно повлиять на первые признаки старения.
Уникальная способность кожи к восстановлению всегда привлекала пристальное внимание ученых. Тонкая грань в этом защитном барьере между окружающей средой и организмом может стать по-настоящему уязвимой, поэтому реакция кожи на повреждения всегда наступает незамедлительно. Сигналом к таким восстановительным работам становится любое травмирующее воздействие (даже обычные отшелушивающие процедуры). Тем не менее, помимо восстановления, в коже непрерывно протекают процессы постоянного обновления.
Новейшая косметология, учитывая особенности физиологического механизма восстановления кожи, может выступить в качестве своеобразной машины времени, искусственно вернув все в исходную «точку разрушения» и далее заставив кожу начать процессы заново, но уже на ином, более качественном уровне.
Стволовые клетки
Одним из важнейших и непременных условий успешного восстановления кожи является наличие в ней функционально активных стволовых клеток. Что же представляют собой эти волшебные стволовые клетки и как они способствуют регенерации, поворачивая время вспять?
Стволовыми называют клетки, которые изначально не имеют каких-либо признаков специализации, попросту говоря - ничего в организме полезного не делают, обладают очень низкой метаболической активностью и очень редко делятся, имеют колоссальную по сравнению с остальными продолжительность клеточного цикла. И лишь при настоятельной необходимости стволовые клетки «просыпаются» и начинают оформляться и делать конкретно то, что организму нужнее всего, приобретая черты и особенности обычных клеток. Именно поэтому они многократно дольше всех остальных клеток остаются «молодыми», представляя собой «золотой резерв» обновления кожи.
До тех пор, пока стволовые клетки кожи сохраняют свою способность к размножению и функциональность, сохраняется и возможность омоложения кожи за счет их дополнительной активации. Например, кроме рутинного обновления, стволовые клетки также активируются в случае ранений и других глубоких повреждений кожи. Однако, скорость естественного обновления кожи, как и скорость заживления ран, с возрастом существенно снижается. ДНК любой клетки на конце имеет определенный участок - теломеру, не содержащий генетической информации, и с каждым делением эта теломера укорачивается.
Ученый Л. Хейфлик, проведя множество экспериментов на клеточных культурах, обнаружил, что в среднем клетки делятся порядка 50 раз, после чего неизбежно гибнут, так как когда теломера заканчивается, укорачиваться начинает уже функциональная часть ДНК и новые клетки получаются уже не «молодыми», а с множеством дефектов и патологий. Тем не менее, более поздние исследования показали, что дело скорее даже не в количестве делений, а в том, что стволовые клетки не получают нужных сигналов от своей стареющей «ниши», и необходимо создать условия, которые могли бы встряхнуть «задремавшие» стволовые клетки и пробудить их нерастраченные пролиферативные резервы.
Цитокины и факторы роста
Цитокины и факторы роста (специализированные сигнальные пептиды) запускают программу отстройки коллагенового каркаса кожи и параллельно (в случае наличия повреждения) позволяют восстановить разрушенные компоненты.
Сигнальные пептиды имеют неоценимое значение в современной косметологии. Среди таких пептидов существует отдельная группа - факторы роста. Именно они принимают непосредственное участие в процессах как физиологической регенерации (естественного обновления тканей), так и репарации (восстановления ткани после повреждения).
В косметике нового поколения уже начали использовать препараты, содержащие цитокины. Однако, было выяснено, что помимо факторов роста в готовые препараты целесообразно включать вещества, необходимые клеткам для метаболизма, так как. во время роста их потребность в питательных веществах сильно возрастает.
Как правильно подходить к вопросам омоложения?
Важно учитывать, что внутри самого организма может присутствовать ряд препятствий к восстановлению кожи, например, ухудшенное кровообращение из-за которого как замедляется вывод токсинов, так и снижается скорость доставки «клеток-ремонтников» к поврежденным местам. Не стоит ограничиваться только одной заветной баночкой с сигнальными пептидами в погоне за вечной молодостью. К решению вопроса омоложения всегда нужно подходить комплексно, реально оценивая потребность в дополнительных средствах и процедурах.
В каком возрасте можно применять такие средства?
В среднем, косметику с факторами роста имеет смысл применять в старшем возрасте, не ранее 35 лет, поскольку молодым девушкам подобного рода коррекция обычно бывает ни к чему и лучше обратить внимание на другие типы пептидов, улучшающих внешние характеристики кожи, а именно на:
Ремоделирующие пептиды (Matrixyl и Syn-Coll), которые работают на улучшение клеточного матрикса и выравнивание микрорельефа кожи.
Пептиды-миорелаксанты (Argireline), рассчитанные прежде всего на уменьшение мимических морщин, а также способные снимать напряжение с мышц лица.
Пептиды-иммуномодуляторы (Rigin), действующие подобно «гормону молодости», улучшающие качество кожи.
Пептиды-активаторы (Eyeseryl и Eyeliss), способные регулировать проницаемость сосудистой стенки, а также уменьшать отечность тканей.
Стоит также помнить о том, что для сохранения молодости кожи, желательно придерживаться здорового образа жизни: правильно питаться, избегать вредных привычек, регулярно заниматься спортом, а также не забывать пользоваться солнцезащитными средствами в период солнечной активности.
В журнале Cell Stem Cell группы китайских ученых. По словам авторов, им удалось впервые в истории получить «в пробирке» сперматозоиды из стволовых клеток. Основные авторы статьи Цюань Чжоу, Мэй Ван, Янь Юань, Сяоян Чжао, Цзяхао Ша и Ци Чжоу. Работают исследователи в лаборатории стволовых клеток и репродуктуивной медицины Института зоологии Китайской академии наук в Пекине и лаборатории репродуктивной медицины Нанкинского медицинского университета.
Заставить стволовые клетки дифференцироваться в соматические клетки определенного типа всегда непростая задача, а уж получить из них половые клетки особенно сложно. Достижения пока невелики. В 2003 году в Пенсильванском университете из стволовых клеток были получены яйцеклетки мышей, но из этих яйцеклеток не смогли получить развивающиеся эмбрионы. В 2012 году также из мышиных эмбриональных стволовых клеток исследователи из Университета Киото получили яйцеклетки и добились рождения из них здоровых мышат. Наконец, в 2014 году ученые из Кембриджского университета и израильского Института Вейцмана сумели получить клетки-предшественники половых клеток человека из клеток кожи, при помощи регуляции работы определенных генов, но по причинам этического и юридического характера не стали продолжать эксперимент.
Со сперматозоидами успехи еще скромнее, чем с яйцеклетками. Команда из Университета Киото в 2011 году смогла из стволовых клеток получить клетки, похожие на предшественники сперматозоидов, но добиться, чтобы эти клетки прошли весь дальнейший путь превращения в сперматозоиды, им не удалось.
Теперь же китайские ученые сообщают, что сумели не только заставить клетки пройти полный цикл сперматогенеза, но и вырастили в результате сперматозоиды, которыми экстракорпорально оплодотворили лабораторных мышей и получили от них здоровое потомство (мышата на заглавной иллюстрации). Достижение это настолько впечатляет, что даже не все специалисты верят, что оно осуществилось в полной мере. Если же дела обстоят действительно так, как сообщается в публикации, то надо признать, что ее авторы станут вероятными кандидатами на получение Нобелевской премии.
Почему же сделать из стволовых клеток клетки половой линии особенно сложно? Чтобы понять это, давайте посмотрим, как образуются сперматозоиды в живом организме. Напомним в начале, что большинство клеток организма (соматические клетки) при делении удваивают свои хромосомы, которые затем расходятся поровну по двум возникающим клеткам. Такой тип деления называется митозом. А половые клетки возникают в результате мейоза, при котором новые клетки получают только половину наследственной информации родительской клетки.
Источником будущих сперматозоидов служат первичные половые клетки (гоноциты). Они возникают еще у эмбриона, не имеющего пока половых желез. Поэтому местом из первичного обитания служит желточный мешок - эмбриональный орган, который у человека работает до конца первого триместра беременности, а потом редуцируется. Образовавшись в желточном мешке, гоноциты потом совершают миграцию через его стенки и попадают туда, где начинают формироваться половые железы. Там они остаются до наступления пубертатного возраста, когда и начинается собственно сперматогенез - образование сперматозоидов.
В мужских семенных железах образование сперматозоидов происходит в семенных канальцах, общая длина которых в организме достигает километра. Созревающие сперматозоиды располагаются на стенках этих канальцев вместе с клетками Сертоли - соматическими клетками, обеспечивающими питание созревающих сперматозоидов и доставку необходимых для этого процесса гормонов. На созревание сперматозоида человека требуется 72 дня. В начале этого процесса гоноцит, сохранившийся с того времени, как организм был эмбрионом, делится митотически, то есть без уменьшения числа хромосом. У двух получившихся клеток разная судьба. Только одна из них превратится в сперматозоид, а вторая так и останется гоноцитом, так что число гоноцитов со временем не сокращается (то есть растратить весь запас сперматозоидов человек никогда не сможет).
Проследим судьбу будущего сперматозоида дальше. Клетка еще три - пять раз поделится митозом, а затем наступит пора двух мейотических делений. Перед первым мейозом клетку называют сперматоцитом первого порядка, перед вторым - сперматоцитом второго порядка, а по завершении второго мейоза - сперматидом. За это время делящиеся клетки при помощи клеток Сертоли постепенно перемещаются из толщи стенки семенного канальца к его просвету. Есть тут и еще одна хитрость: во время миотозов и даже после первого мейоза клетки при делении не отрываются друг от друга полностью, а остаются связанными цитоплазматическими мостиками. Это нужно, во-первых, для обеспечения высокой синхронности деления, а во-вторых, из-за того, что многие белки, задействованные в сперматогенезе, связаны с генами, которые расположены на половых хромосомых (и на X, и на Y), а после мейоза, как мы помним, в клетке останется только одна из этих хромосом.
После второго мейоза сперматид приобретает характерную форму. У него почти полностью исчезает цитоплазма, зато образуются важные для сперматозоида органы: жгутик для движения и акросома, которая в будущем должна помочь ему растворить оболочку яйцеклетки. После этого будущий сперматозоид должен еще дозреть, и лишь после этого он будет готов к использованию. Также для нормального развития эмбриона после оплодотворения важно, чтобы хромосомы в сперматозоидах имели определенный «профиль метилирования», то есть к определенным участкам молекулы ДНК присоединены метильные группы (CH 3), которые влияют на работу генов.
Ученый, желающий получить сперматозоиды из стволовых клеток в лаборатории, должен ухитриться воспроизвести все необходимые условия разных стадий сперматогенеза, заставить включаться и выключаться в нужный момент определенные гены, обеспечить необходимые гормоны (опять-таки на разных стадиях - разные), контролировать характеристики среды, в которой растут клетки.
Чтобы добиться успеха, китайские исследователи применили ряд цитокинов , которые близки сигнальным молекулам, определяющим развитие эмбриона на начальных стадиях. В результате взятые для эксперимента эмбриональные стволовые клетки мышей удалось дифференцировать в эпибластоподобные клетки, то есть похожие на клетки желточного мешка, а затем и в гоноцитоподобные клетки. В дальнейшем авторы работы выращивали гоноцитоподобные клетки вместе с клетками эпителия семенных желез новорожденных мышей. Такой состав среды, по их мнению, наиболее точно воспроизводит ситуацию в семенных железах живой мыши. Затем в эту среду надо было добавлять вещества, которые направляли развитие гоноцитоподобных клеток в нужную сторону, а также необходимые гормоны. По словам авторов, им пришлось проделать сотни экспериментов, прежде чем они подобрали все нужные компоненты и установили необходимый порядок этих действий. Им удалось вовремя заставить клетки перейти от митоза к мейозу.
Схема эксперимента
Итогом всей этой работы стали все-таки не сперматозоиды в полном смысле слова, а похожие на незрелые сперматозоиды клетки, лишенные жгутика и акросомы. Зато у них сохранялись клеточные органы, которые у нормальных сперматозоидов отсутствуют. Все развитие клеток от гоноцитоподобных до сперматидоподобных занимает 14 дней.

Сперматидоподобные клетки, полученные китайскими учеными
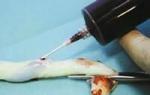
Самостоятельно такие клетки не смогли бы оплодотворить яйцеклетку, но ученые применили метод ICSI (intracytoplasmic sperm injection) - интрацитоплазматической инъекции сперматозоида в яйцеклетку. В данном случае сперматозоид попадает прямо в цитоплазму яйцеклетки при помощи специальной иглы. Оплодотворенные полученными клетками яйцеклетки были имплантированы в матку мыши, и в итоге родились шесть мышей. Сейчас они уже сами произвели потомство.
Часть ученых воспринимает сообщение об этом открытии с большим скептицизмом. Митинори Саитоу, который возглавляет группу Университета Киото, впервые получившую гоноцитоподобные клетки, отмечает, что ряд моментов в статье показали ему странными. Например, китайские исследователи культивировали клетки при температуре 37° C, что примерно на три градуса выше температуры, при которой происходит нормальный сперматогенез. Также он отмечает, что в гоноцитоподобных клетках, полученных в Китае, не отмечается всех белков, необходимых для данного типа клеток, что ставит под сомнение возможность вырастить из них сперматозоиды. Вызывает сомнение неожиданное ускорение развития клеток. Как уже говорилось, в клеточной культуре сперматидоподобные клетки были получены за 14 дней, тогда как в живой мыши этот процесс занимает больше четырех недель. Такехико Огава, специалист по биологии развития из Университета Иокогамы, намерен повторить эксперимент китайских ученых с целью проверки их результатов. Один из руководителей китайского коллектива, Ци Чжоу, в ответ на такие намерения утверждает, что протокол их эксперимента вполне воспроизводим в других лабораториях. Сами же китайские исследователи планируют перейти к экспериментам на человеческих стволовых клетках.
Даже при условии, что полученные результаты окажутся воспроизводимыми, клиническая перспектива нового метода остается далекой. Различие между человеком и мышью довольно значительны, и выявленный «рецепт» выращивания сперматозоидов из стволовых клеток мыши для человеческих сперматозоидов не подойдет.